A sók okozta épületkárok fajtái és keletkezésük
Só alatt elsősorban olyan vegyületeket értünk, amelyek savak és bázisok egymással való vízkilépéssel járó reakcióinak termékei. Ilyenkor a bázis fémionja lép a sav hidrogénionjának helyébe. Savak hatására a kötőanyag fémje (túlnyomórészt kalcium) jól oldható anyaggá alakul át, amelyet aztán a talajvíz, a szivárgó víz vagy az esővíz kiold az építőanyagokból. Ezáltal fellazul az építőanyag szerkezete, ill. károsodik a kötőanyag. Az előforduló savak rendszerint: salétromsav, kénsav, sósav és szénsav. A salétromsav nitrózus gázokból vagy ammónia és szerves nitrogénvegyületek (vizelet, fehérje stb.) lebontása során keletkezhet.
A sók kárai
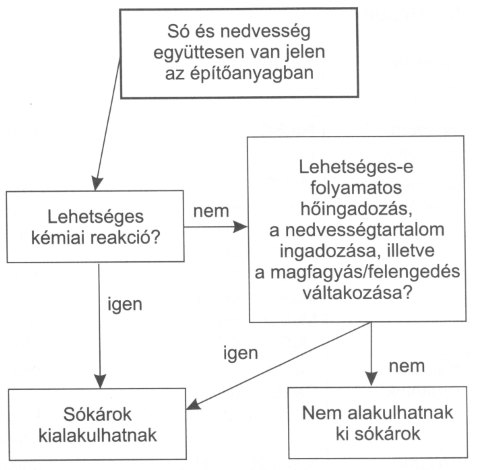
Ahhoz, hogy a sók valamilyen formában károkat okozhassanak, kémiai vagy fizikai folyamatokban el kell reagálniuk az építőanyaggal, vagy más típusú kölcsönhatásban kell részt venniük. Nagy sóterhelésű építőanyagok helyreállítása során megkülönböztetett módon kell eljárni. Fontos tudnunk arról, hogy a sók kristályosodása és hidratációja repesztő hatást idézhet elő, és hogy a higroszkópos sók néha olyan hatások látszatát keltik, amelyek a valóságban nincsenek is jelen!
Ha ismerjük a sókban rejlő veszélyeket, a helyreállítás során használt anyagoknál utána kell nézni, ellenőrizni kell és meg kell vizsgálni, hogy a munkálatok során keletkezhet-e új sófajta. Ha egy objektumot helyre kell állítani, elsősorban annak kell világosnak lennie, hogy mely sók vannak jelen, honnan származik a nedvesség, és hogy milyen mértékben vannak jelen a sók, ill. a nedvesség.
A sók okozta épületkárok fajtái és keletkezésük
A sók különféle károkat okozhatnak az épületeken. Ezek egy része korlátozódhat a felszínre (foltos sókiválás és a felület korróziója), a többi viszont a fal teljes terjedelmét érinti, és adott esetben mélyreható károkat vagy akár teljes szétroncsolódást idézhet elő.
A sók felszíni megjelenését gyakran ártalmatlannak vélik, inkább csak olyasminek tekintik, ami esztétikailag zavaró, optikailag rontja a homlokzatok, lábazatok vagy pincefalak megjelenését. Ilyenkor a felszíni sófelhalmozódás általában a falon belüli sómozgásra utal, és olyan mélyebb rétegekben végbemenő folyamatok első indikátora lehet, amelyek jelentős kockázatot jelenthetnek a fal állapotára nézve. Annak ellenére, hogy a sókéreg csapadék után gyakran szemmel láthatóan, nyomok visszamaradása nélkül eltűnik, száraz időszakokban rendszerint újra előjön.
Akart okozó sóréteg gyakran nem közvetlenül a felszínen fedezhető fel, hanem néhány milliméterrel mélyebben lokalizálódik, és kívülről eleinte egyáltalán nem látható. Ilyen esetben a sókoncentráció annál mélyebbre ható roncsolódáshoz vezet, minél később fedezik fel. A rettegett fekete kéreg jellegzetes példa az ilyen fajtájú sóaktivitásra. Sókérgek nemcsak az épületek külső falán alakulnak ki, hanem a belső terekben is megtalálhatók, és ott is a kültériekkel minden téren hasonló módon jelennek meg.
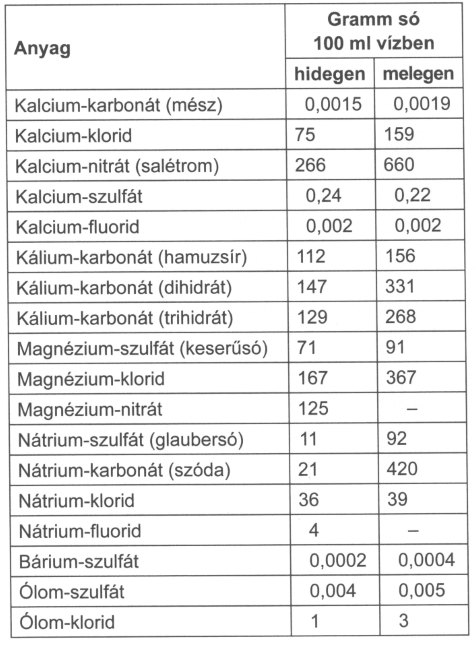
Sók oldhatósága vízben:
Egy sófajta károsító hatásának fontos paramétere a vízoldhatósága, hiszen a vizes transzport túlzott sófelhalmozódáshoz, az pedig roncsoló hatásokhoz vezet.
A specifikus, az építőanyag és a környezet összetételéből egyértelműen következő reakciók mellett molekuláris síkon nagy jelentőségű mindenekelőtt a fagy hatása, az oldhatóság eltolódása és a csapadékképző reakciók. Ilyenkor megfigyelhető, hogy a sók és a sóoldatok oldódási, kristályosodási, fagyási és csapadékképző viselkedése az ásványi anyagokra jellemző szűk pórusrendszerben a szabad anyagok viselkedésétől lényegesen eltérhet.
Ezenkívül gyakorta megfigyelhető kettős sók vagy komplex összetételű keveréksók képződése. A kettős sók képződésének lehetősége miatt a különböző sókat együttesen tartalmazó sóoldatokból az építőanyagok vízzel részlegesen telített pórusaiban igen komplex többanyagú-többfázisú rendszerek alakulnak ki, amelyek viselkedése jelen pillanatban még semmi esetre sem tekinthető tisztázottnak.
A sók fajtái és gyakorisága
A köznyelvben a só kifejezés alatt a vegyületcsoport egyik tagját, a konyhasót értik. Ez a sófajta a természetben összességében domináns szerepet játszik ugyan, azonban az építményekben csak mellékesen fordul elő. Nála sokkal gyakoribbak más típusú sók, amelyek sokszínűsége és oldataik változó töménysége újra és újra meglepetéssel szolgál. A kloridok, mint a nátrium-klorid is, viszonylag ritkák, túlnyomó többségében szulfátok fordulnak elő, őket követik a nitrátok és a karbonátok.
Ezenkívül mutattak már ki foszfátokat (pl. apatit, strengit, foszfosziderit, ludlamit, vivianit vagy metavivianit), fluoridokat (pl. carobbiit, villiaumit vagy fluorit), fluoroszilikátokat (pl. mailadrit vagy hieratit) vagy oxalátokat (pl. whewellit vagy weddellit).
A sók káros hatása főként arra vezethető vissza, hogy a megjelenő nedvesség (pl. kapillárisán felszálló nedvesség) hatására beoldódnak, és a későbbi kiszáradás során nagy mennyiségű víz, az ún. kristályvíz megkötése mellett kikristályosodnak. A vízfelvétel a képződő kristályok térfogatának növekedését eredményezi, ez pedig kristályosodási nyomást idéz elő. Oldható sók jelenléte olyankor is káros lehet, ha azok az építőanyag mésztartalmával vízoldható vegyületté alakulnak, ezáltal kioldják a kötőanyagot, az mészben szegényedik.
A mészben szegényedés a kikristályosodással szemben csak olyan épületelemekben játszódhat le, amelyek hosszabb időn keresztül nedves állapotban voltak. Attól függetlenül, hogy a kioldódás okozta károk lényegesen lassabban alakulnak ki, mint azok, amelyek a kristályosodás hatására jönnek létre, idővel ezek is jelentős szétroncso-lódáshoz vezetnek.
Ebből az következik, hogy csak olyan sóknak lehet épületkárosító hatása, amelyek vízben vagy gyengén savas vizes oldatban oldódnak. Utóbbihoz tartozik a talajvízen kívül az esővíz is, mivel az egyrészt szénsavat vesz fel a levegőből, másrészt pedig kén-dioxidot köt meg a füstgázokból, nitrózus gázokat pedig a kipufogógázokból. Ezzel szemben az oldhatatlan sók nem károsítják az épületeket, így ebből a szempontból teljesen érdektelenek.
Fontos!
Kristályosodási nyomás
Porózus építőanyagok kiszáradása során, ha elegendően magas a pórusokban található oldat koncentrációja, sókristályok képződnek (kikristályosodás). Ha a kristályképződést gátolja a pórusgeometria, akkor túlnyomás alakul ki a pórusszerkezeten belül. Ha folyamatosan váltakozik a sók kikristályosodása és beoldódása, akkor az törvényszerűen szétroncsolja az építőanyagot.
Kristályosodó sók miatt háromféle mechanizmus szerint keletkezhetnek károk:
- hidrosztatikus kristályosodási nyomás, vagy kristályosodási nyomás túltelített oldat miatt;
- lineáris növekedési nyomás;
- hidratációs nyomás.
A szakirodalom nem különíti el egyértelműen egymástól a kristályosodási nyomást és a lineáris növekedési nyomást, így gyakran mindkét fogalom ugyanarra a jelenségre utal.
Mint minden kristály, az oldatból kiváló kristályok is csak az őket határoló kristályfelületek mentén növekedhetnek. Az ásványi építőanyag pórustere gátolhatja a sókristályok szabad növekedését, ha a növekvő kristály a pórus szemben lévő falával találkozik, vagy ha a kristályok kölcsönösen akadályozzák egymást. Ez a jelenség különösen tű, henger vagy rúd alakú kristályoknál figyelhető meg, tehát amelyeknél az egyik növekedési irány különösen előnyben részesített.
Nedvességgel és sókkal terhelt falaknál a károsodás lehetősége főként abban áll, hogy a sók kikristályosodása, tehát az a folyamat, amelynek során oldott állapotból szilárd fázisúvá alakulnak, jelentős térfogat-növekedéssel jár. Ha a térfogatnövekedés nem tud kiegyenlítődni vagy eloszlani az építőanyag szerkezetén belül, kialakul az ún. kristályosodási nyomás.
Ez azt jelenti, hogy a kapilláristerekben és az építőanyag pórusaiban megtalálható túltelített sóoldat térfogata nedvesség leadásával növekszik, és kristályosodási nyomást fejt ki a pórusok falára. Ilyenkor az a törvényszerűség érvényes, hogy minél több kristályvizet vesz fel egy só, annál nagyobb a kristályosodási nyomás károsító hatása. Továbbá a folyamat hőmérsékletfüggést is mutat. Ha folyamatosan váltakozik az átnedvesedés és a kiszáradás, az felerősíti a folyamatot.
A kristályosodási nyomás feszítő hatást fejt ki, mértéke többszörösen meghaladja az építőanyag szilárdsági tulajdonságait, így az anyag kezdetben elporlad, utána pedig sókivirágzások és/ vagy lerepedezések keletkeznek. A sókristályok növekedéséből adódó nyomást általában kristályosodási nyomásnak nevezik, holott a lineáris növekedési nyomás elnevezés jobban kifejezné a jelenség mibenlétét.
Például nátrium-szulfát vizes oldatából 32,4 °C-ig a 10 kristályvizet tartalmazó mirabilit (Na2S04* 10H2O) kristályosodik ki, 32,4 °C felett pedig a kristályvízmentes thénardit (Na2S04). Az átkristályosodás csak nátrium-szulfát-oldat jelenlétében mehet végbe. A gyakorlatban ilyen ritkán esik meg. Legtöbbször további ionok, mint pl. magnézium stb. ionok együttesen vannak jelen. Magnézium jelenlétében már 15 °C-on a vízmentes nátrium-szulfát képződik. Mivel a kikristályosodás csak olyan épületrészekben mehet végbe, amelyek az idő túlnyomó részében szárazak, a tartósan nedves vagy vízben álló épületelemeket nem károsítják a sók.
A kristályosodáskor kialakuló nyomást befolyásolja a pórusok sugarának eloszlása. Azt tételezzük fel, hogy a pórusszerkezet terhelése során nem az egyszeri kikristályosodás fejt ki roncsoló hatást, hanem az ismétlődő ciklusok. Ehhez járul még, hogy kristályok inkább a nagyobb pórusokban, üregekben és repedésekben képződnek, miközben a sóoldat a finom pórusokból odaáramlik. A pórusrendszer belsejében a növekedő jégkristályokról alkotott modellel analóg módon feltételezhető, hogy a kisebb pórusokban kialakuló kristálynak nagyobb a kémiai potenciálja, mint a nagyobb pórusban növekvőnek. Eszerint a legnagyobb kristályosodási nyomásnak mindig a nagyrészt finom pórusokat tartalmazó építőanyagokban kellene kialakulnia.
Meglepően gyakran találkozhatunk ún. kettős sókkal. Ezek egynél több kationból és anionból állnak. Az is különös, hogy sok sófajta különböző mértékben lehet hidratált. Ez a tény a sók metamorfózisa és repesztő hatása miatt fontos. Az oldatok telítési koncentrációját is befolyásolja, hogy mely hidrátformáról van szó.
A só vízmegkötése
A kristályképződés lehetősége mellett néhány sónak van olyan tulajdonsága, hogy bizonyos hőmérséklet-tartományban vizet köt meg a kristályrácsában, ill. vizet ad le onnan. Ezt a folyamatot hidratációnak nevezik, és a víz megkötése szintén térfogat-növekedéssel jár. Ez annyit tesz, hogy bizonyos sók esetén, ha azok túltelített oldatukból kristályosodnak ki, térfogat-növekedés figyelhető meg.
Ilyenkor a túltelített oldatnak kisebb a térfogata, mint a kiváló sókristályoknak és a visszamaradó telített oldatnak együttesen. Ha a túltelített oldat teljesen kitölt egy adott pórust, és a képződő kristályok elzárják a pórusok kijáratait, akkor a pórus falára minden irányból hat hidrosztatikai nyomás. Egyes sók már 40 °C körül leadják a kristályvizüket, ill. már ilyen hőmérsékleten képesek vizet felvenni, ha csökken a hőmérséklet vagy nő a páratartalom.
A sók eredete
A mindennemű sószennyezéstől mentes falak ritkák, még ha a sók jelenléte nem is jelent feltétlenül sók általi károkat. Mivel a sók általában jelen vannak, felmerül a kérdés, hogy hogyan is kerültek oda. Eredetük különböző lehet. Ott lehetnek az eredeti építőanyagban (építőelemek, kötőanyag, adalékanyag, adalékvíz), de kívülről is bejuthatnak (talajvízzel vagy csapadékkal). Ezenkívül sók újonnan is képződhetnek a már létező épületben (cirkuláló víz vagy légszennyező anyagok miatt). Egy figyelemre méltó és nagyon kevéssé szem előtt tartott módja a sók megjelenésének, amikor javítási munkálatok során kerülnek az addig kevéssé szennyezett építménybe, majd ott kifejtik romboló hatásukat, ami a javítás nélkül nem lett volna lehetséges.
Az építőanyagok sóval való szennyezettsége
Sok építőanyag természetszerűleg tartalmaz sókat. Ez különösen jellemző a természetes kőzetekre, de ilyenek a kerámiák és a téglák is. Ezekben jelentős mennyiségben lehetnek jelen épületkárosító sók. Potenciális sóhordozók a természetes kövek (homokkő, pala, szürkekavics) éppúgy, mint a mesterségesen előállítottak (pl. téglák). Az eredetnek és a nyersanyagnak megfelelően akár jelentős sóterhelésről is szó lehet.
Ezt különösen az olyan építőköveknél kell figyelembe venni, amelyek maguk is sókból állnak, ilyen pl. a gipsz, a mészkő vagy az anhidrit. A kötőanyag nagyon gyakran okoz sószennyezést. A műemlékek mészhabarcsa mindenesetre ritkán tekinthető ilyen típusú sóforrásnak, mivel lényegében csak kalcium-karbonátból áll. Az adalékok viszont, mint pl. a hidraulikus anyagok, figyelemre méltó mennyiségben tartalmazhatnak más oldható sókat vagy ezek lehetséges alkotórészeit.
A vulkáni eredetű trassz vagy puccolán nagyon bőséges források, de az agyagtól nem megfelelően megtisztított mész is jelentősen hozzájárulhat a sóterheléshez. A gipszhabarcsok legnagyobb részét egy könnyen mozgósítható só, a gipsz teszi ki. A gipsz meglepően jól oldódik, 1 1 20 °C-os víz 2 g-ot képes beoldani, ezáltal könnyen átkerülhet a fal egyik részéből a másikba. Ha más sóképzőkkel találkozik, másodlagos reakciók mehetnek végbe. Ilyen pl. a viszonylag gyakran megfigyelhető szingenitképződés. Ezért, ha a műemlékek vagy történelmi épületek falai tartalmaznak gipszhabarcsot vagy gipszvakolatot, akkor különösen elővigyázatosan kell eljárni!
Az oldhatatlan sók nem igazán veszélyesek, azonban azok, amelyek vízben vagy vizes oldatokban (pl. savak) oldhatók jelentős épületkárokat okozhatnak. Ez érvényes az olyan nehezen oldhatónak vélt sókra is, mint pl. a kalcium-szulfát vagy -karbonát. Ezek oldhatósága még mindig elég magas ahhoz, hogy jelentős veszélynek tegyék ki az épületeket.